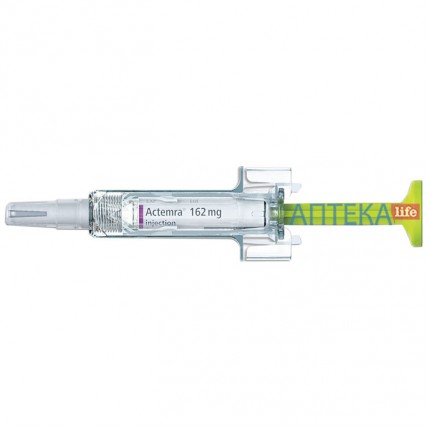
Где купить АКТЕМРА® раствор д/ин., 162 мг/0,9 мл в предвар. запол. шпр. №4
Аптека 7Я №1
Аптека 7Я+ №1
ІНСТРУКЦІЯ
для застосування медичного імунобіологічного препарату
АКТЕМРА®
(АCTEMRA®)
Склад:
діюча речовина: tocilizumab;
1 попередньо наповнений шприц містить тоцилізумабу 162 мг/0,9 мл;
допоміжні речовини: полісорбат 80, L-аргінін, L-аргініну гідрохлорид, L-метіонін, L-гістидин, L-гістидину гідрохлориду моногідрат, вода для ін’єкцій.
Лікарська форма. Розчин для ін’єкцій.
Основні фізико-хімічні властивості: рідина від прозорої безбарвної до злегка жовтуватої, сильно опалесціюючої, з величиною опалесцентності не більше 30,0 турбідиметричних одиниць за формазином, забарвлена не інтенсивніше ніж еталон Y4.
Фармакотерапевтична група.
Імуносупресанти, інгібітори інтерлейкіну.
Код АТХ L04А C07.
Фармакологічні властивості.
Фармакодинаміка.
Тоцилізумаб – рекомбінантне гуманізоване моноклональне антитіло, дія якого спрямована до людських розчинних та мембранних рецепторів інтерлейкіну-6 (ІЛ-6) з підкласу імуноглобулінів G1 (IgG1).
Механізм дії
Тоцилізумаб специфічно зв’язується як з розчинними, так і з мембранними рецепторами ІЛ-6 (sIL-6R і mIL-6R). Продемонстровано, що тоцилізумаб інгібує sIL-6R і mIL-6R-опосередковані сигнали. ІЛ-6 є багатофункціональним прозапальним цитокіном, що виробляється різними типами клітин, включаючи Т- і В-клітини, моноцити та фібробласти. ІЛ-6 залучений у різноманітні фізіологічні процеси, такі як стимуляція секреції імуноглобулінів, активація Т-клітин, стимуляція продукування білків гострої фази в печінці та стимуляція гемопоезу. ІЛ-6 залучений в патогенез різних захворювань, у тому числі запальних захворювань, остеопорозу та новоутворень.
Фармакодинамічні ефекти
У клінічних дослідженнях тоцилізумабу спостерігалося різке зменшення рівнів С-реактивного білка (CPБ), швидкості осідання еритроцитів (ШОЕ) і амілоїду А в сироватці крові (СAA). Відповідно до впливу на реагенти гострої фази лікування тоцилізумабом було пов’язано зі зменшенням кількості тромбоцитів в межах нормального діапазону. Спостерігалося підвищення рівня гемоглобіну завдяки дії тоцилізумабу, яке призводило до зменшення ефекту IЛ-6 на продукування гепсидину, і, в свою чергу, до збільшення наявності заліза. У пацієнтів, яких лікували тоцилізумабом, вже на другий тиждень спостерігалося зменшення рівнів CPБ до меж норми, яке підтримувалося протягом лікування.
У здорових добровольців, яким призначався тоцилізумаб у дозах від 2 до 28 мг/кг внутрішньовенно і від 81 до 162 мг підшкірно, абсолютне число нейтрофілів знизилося до найнижчого рівня на 2-5-й день після призначення. Згодом число нейтрофілів поверталося до вихідного рівня, що залежало від дози. Пацієнти з ревматоїдним артритом (РА) після призначення тоцилізумабу демонструють, порівняно із здоровими людьми, зниження абсолютного числа нейтрофілів.
Ефективність тоцилізумабу при введенні підшкірно у послабленні симптомів РА та рентгенологічну відповідь оцінювали у двох рандомізованих, подвійних сліпих, контрольованих, багатоцентрових дослідженнях. У дослідження І (ПШ-І) були включені пацієнти віком > 18 років з помірним або тяжким активним РА, діагностованим відповідно до критеріїв Американської колегії ревматологів (AКР), які мали на початку дослідження принаймні 4 суглоби з болем і 4 суглоби з набряком. Всі пацієнти отримували базову небіологічну терапію захворювання-модифікувальними протизапальними препаратами (ЗМПП). Для дослідження II (ПШ-II) були залучені пацієнти віком > 18 років з помірним або тяжким активним РА, діагностованим відповідно до критеріїв AКР, які мали на початку дослідження принаймні 8 суглобів з болем і 6 суглобів із набряком.
Переведення з внутрішньовенного введення 8 мг/кг один раз на 4 тижні на підшкірне застосування 162 мг один раз на тиждень впливає на експозицію в пацієнта. Ступінь зміни залежить від маси тіла пацієнта (збільшена у пацієнтів з малою масою тіла та зменшена у пацієнтів з великою масою тіла), але клінічний результат відповідає такому, що спостерігався у пацієнтів при внутрішньовенному введенні.
Фармакокінетика.
Фармакокінетичні параметри тоцилізумабу оцінювалися за допомогою популяційного фармакокінетичного аналізу бази даних 1759 пацієнтів з ревматоїдним артритом, які отримували підшкірну ін’єкцію тоцилізумабу у дозі 162 мг 1 раз на тиждень, 162 мг 1 раз на 2 тижні або 8 мг/кг внутрішньовенно кожні 4 тижні протягом 24 тижнів.
Фармакокінетичні параметри тоцилізумабу не змінювалися залежно від часу. Для тоцилізумабу у дозі 162 мг 1 раз на тиждень прогнозована середня (± стандартне відхилення) AUC1тиждень в рівноважному стані становила 8200 ± 3600 мкг•год/мл, Cmin і Cmax – 44,6 ± 20,6 мкг/мл та 50,9 ± 21,8 мкг/мл відповідно. Коефіцієнти накопичення для AUC – 6,83, Cmaх і Cmin – 6,37 та 5,47 відповідно. Було досягнуто рівноважного стану для Cmax, AUC і Cmin після 12 тижнів.
Для тоцилізумабу у дозі 162 мг 1 раз на 2 тижні прогнозована середня (± стандартне відхилення) AUC2тижні в рівноважному стані становила 3200 ± 2700 мкг•год /мл, Cmin і Cmax – 5,6 ± 7,0 мкг/мл та 12,3 ± 8,7 мкг/мл відповідно. Коефіцієнти накопичення для AUC – 2,67, Cmin і Cmaх – 5,6 та 2,12 відповідно. Було досягнуто рівноважного стану для AUC і Cmin після 12 тижнів та для Cmax після 10 тижнів.
Абсорбція
У пацієнтів з ревматоїдним артритом після підшкірного введення час до досягнення піка максимальної концентрації в сироватці крові (tmax) cтановив 2,8 дня, а біодоступність – 80 %.
Виведення
При застосуванні препарату у вигляді підшкірної ін’єкції період напіввиведення (t1/2) залежить від концентрації і при дозуванні 162 мг 1 раз на тиждень у пацієнтів з РА в рівноважному стані становить до 13 днів, а при застосуванні 162 мг 1 раз на 2 тижні – 5 днів.
Особливі популяції
Пацієнти з порушенням функції нирок: офіційні дослідження фармакокінетики тоцилізумабу у пацієнтів з порушенням функції нирок не проводилися. Більшість пацієнтів у популяційному фармакокінетичному аналізі мали нормальну функцію нирок або порушення функції нирок легкого ступеня тяжкості (кліренс креатиніну за формулою Кокрофта – Голта < 80 мл/хв та ≥ 50 мл/хв), що не впливало на фармакокінетику тоцилізумабу.
Пацієнти з порушенням функції печінки: офіційні дослідження фармакокінетики тоцилізумабу у пацієнтів з порушенням функції печінки не проводилися.
Стать, раса, вік: популяційний фармакокінетичний аналіз пацієнтів з ревматоїдним артритом показав, що вік, стать і раса не впливають на фармакокінетику тоцилізумабу.
Клінічні характеристики.
Показання.
Застосування препарату Актемра® в комбінації з метотрексатом (МТ) показано для лікування активного ревматоїдного артриту (РА) помірного або тяжкого ступеня у дорослих пацієнтів, у яких спостерігалася неналежна відповідь або непереносимість попередньої терапії одним або більше захворювання-модифікувальним протизапальним препаратом (ЗМПП) або антагоністом фактора некрозу (ФНП) пухлини. Таким пацієнтам препарат Актемра® можна призначати у вигляді монотерапії у випадку непереносимості метотрексату або якщо продовжувати лікування метотрексатом недоцільно.
При застосуванні в комбінації з метотрексатом препарат Актемра® гальмує прогресування деструктивних змін у суглобах, за рентгенологічними даними, та покращує фізичну функцію.
Протипоказання.
Гіперчутливість до тоцилізумабу або будь-якого іншого компонента препарату.
Активні, тяжкі інфекції.
Взаємодія з іншими лікарськими засобами та інші види взаємодій.
Дослідження взаємодії проводилося лише у дорослих пацієнтів.
Одночасне одноразове введення тоцилізумабу у дозі 10 мг/кг і метотрексату у дозі 10-25 мг 1 раз на тиждень суттєво не впливало на експозицію метотрексату.
Популяційний фармакокінетичний аналіз не виявив будь-якого впливу метотрексату, нестероїдних протизапальних препаратів (НПЗП) або кортикостероїдів на кліренс тоцилізумабу.
Утворення печінкових CYP450 ізоферментів пригнічується під впливом цитокінів, таких як ІЛ-6, що стимулюють хронічне запалення. Таким чином, при проведенні терапії засобами, які інгібують дію цитокінів (наприклад тоцилізумаб), експресія ізоферментів CYP450 може бути порушена.
У дослідженні in vitro, проведеному на культурі гепатоцитів людини, було показано, що ІЛ-6 спричиняв зниження експресії ферментів CYP1A2, CYP2C9, CYP2C19 і CYP3A4. Застосування тоцилізумабу нормалізує експресію цих ізоферментів.
Концентрація симвастатину (субстрат CYP3A4) через 1 тиждень після одноразового введення тоцилізумабу у пацієнтів з РА знижувалася на 57 % до аналогічної або дещо підвищеної концентрації симвастатину у здорових добровольців.
На початку чи при закінченні курсу терапії тоцилізумабом необхідно ретельно спостерігати за пацієнтами, які отримують лікарські засоби, що метаболізуються за допомогою ізоферментів CYP450 3A4, 1A2 чи 2C9 в індивідуально підібраних дозах (наприклад аторвастатин, блокатори кальцієвих каналів, теофілін, варфарин, фенпрокоумон, фенітоїн, циклоспорин чи бензодіазепіни). Для забезпечення терапевтичної дії цих препаратів може виникнути потреба у підвищенні їхньої дози. Через тривалий період напіввиведення (t1/2) тоцилізумабу його вплив на активність CYP450 ферментів може зберігатись протягом декількох тижнів після припинення терапії.
Особливості застосування.
Інфекції
У пацієнтів, які отримують імуносупресивні засоби, у тому числі препарат Актемра®, спостерігалися випадки серйозних інфекцій (іноді з летальним наслідком) (див. розділ «Побічні реакції»). Не слід починати лікування препаратом Актемра®пацієнтам з активними інфекційними захворюваннями (див. розділ «Протипоказання»). При розвитку серйозних інфекцій терапію препаратом Актемра® слід припинити до усунення інфекції (див. розділ «Побічні реакції»). Медичним працівникам слід дотримуватися обережності при застосуванні препарату Актемра® пацієнтам із рецидивними або хронічними інфекціями в анамнезі, а також при супутніх захворюваннях, що сприяють розвитку інфекцій (наприклад дивертикуліт, цукровий діабет та інтерстиціальне захворювання легень).
Слід бути особливо пильним з метою своєчасного виявлення серйозних інфекційних захворювань у пацієнтів з помірним або тяжким ревматоїдним артритом, які отримують біологічні препарати, оскільки симптоми гострого запалення можуть бути стертими через пригнічення реакцій гострої фази. Слід враховувати ефекти тоцилізумабу на С-реактивний білок, нейтрофіли, симптоми інфекцій при оцінці можливості розвитку інфекції у пацієнта. Пацієнтів необхідно проінформувати про необхідність негайного звернення до лікаря при виникненні будь-яких симптомів, що свідчать про появу інфекції, з метою своєчасної діагностики та призначення необхідного лікування.
Туберкульоз
Перед призначенням препарату Актемра®, як і при призначенні інших біологічних препаратів для лікування ревматоїдного артриту, необхідно провести попереднє обстеження пацієнтів на наявність латентного туберкульозу. При виявленні латентного туберкульозу необхідно провести стандартний курс антимікобактеріальної терапії перед початком лікування препаратом Актемра®. Лікарям слід пам’ятати про ризик хибно негативних результатів туберкулінового шкірного тесту і результатів гамма-інтерферон-туберкулінового аналізу крові, особливо у тяжкохворих пацієнтів і пацієнтів з імунодефіцитом.
| Особенности | |
| Страна: | ШВЕЙЦАРІЯ |
| ATC – классификация: | L04AC |
| Рецептурное: | Рецепт |
| Срок годности: | 01.01.2050 0:00:00 |
| Форма выпуска: | раствор |
| Номер регистрации: | UA/13909/02/01 |
| Штрих код: | 7 640 149 615 227 |
| Свойства: | Інгібітори інтерлейкіну |