Де купити Бемфола розчин д/ін. 75 МО (5,5 мкг) по 0,125 мл №1 у поперед. запов. руч. з голк. та серв.
Аптечный пункт АЛЬТА-С №1
Пн - Пт з 8:00 до 16:00 Сб - Нд Вихiдний
Аптечный пункт АЛЬТА-С №2
Пн - Пт з 8:00 до 18:00 Сб - Нд Вихiдний
Аптека АЛЬТА-С №3
Пн - Пт з 8:00 до 17:00 Сб - Нд з 9:00 до 14:00
Аптека №3 ТОВ "7Я+"
Пн - Пт з 08.00 до 19.00
Сб з 08.00 до 16.00
Нд - вихідний
ТОВ "7я+"
Аптека
ФАРМАСФЕРА №2
Пн - Пт з 08.00 до 20.00, Сб-НД з 08.00 до 18.00, без вихiдних
Аптека
ФАРМАСФЕРА №3
Аптека
ФАРМЦЕНТР №2
Пн - Пт з 8:00 до 19:00, Сб - з 9:00 до 14:00, Нд - вихiдний
Аптечный пункт ФАРМЦЕНТР №2
Пн - Пт: з 8-00 до 18:00, Сб: з 9-00 до 15:00,Нд: Вихiдний
Аптека 7Я+ №1
Аптека 7Я №1
Склад
діюча речовина: фолітропін альфа*;
1 мл розчину містить 600 МО (44 мкг) фолітропіну альфа;
одна попередньо наповнена ручка містить:
75 МО (5,5 мкг) фолітропіну альфа в 0,125 мл, або
150 МО (11 мкг) фолітропіну альфа в 0,25 мл, або
225 МО (16,5 мкг) фолітропіну альфа в 0,375 мл, або
300 МО (22 мкг) фолітропіну альфа в 0,5 мл, або
450 МО (33 мкг) фолітропіну альфа в 0,75 мл;
* рекомбінантний людський фолікулостимулюючий гормон (р-лФСГ)
допоміжні
речовини: сахароза; натрію гідрофосфат, дигідрат; натрію дигідрофосфат,
дигідрат; L-метіонін; полоксамер 188/ лютрол F-68; кислота фосфорна;
вода для ін’єкцій.
Лікарська форма
Розчин для ін’єкцій в попередньо наповненій ручці.
Основні фізико-хімічні властивості: прозорий безбарвний розчин.
Фармакотерапевтична група
Статеві гормони та модулятори статевої системи. Гонадотропіни. Код ATХ G03G A05.
Фармакологічні властивості
Фармакодинаміка.
Бемфола
– це подібний біологічний лікарський засіб, який містить рекомбінантний
людський фолікулостимулюючий гормон (р-лФСГ) в якості діючої речовини,
отриманий методом генної інженерії з клітин яєчника китайського хом’яка.
Фармакодинамічні ефекти
Найважливішим
ефектом парентерального введення фолікулостимулюючого гормону (ФСГ) у
жінок є розвиток зрілих граафових фолікулів. Метою терапії фолітропіном
альфа у жінок з ановуляцією є формування одного зрілого граафового
фолікула, з якого після введення людського хоріонічного гонадотропіну
(лХГ) вивільниться яйцеклітина.
Клінічна ефективність та безпека застосування для жінок
У
клінічних дослідженнях пацієнтки з тяжкою недостатністю ФСГ та
лютеїнізуючого гормону (ЛГ) визначалися за сироватковим рівнем
ендогенного ЛГ < 1,2 МО/л, отриманим в аналізі центральної
лабораторії. Проте слід взяти до уваги, що рівень ЛГ, визначений у
різних лабораторіях, може відрізнятися.
У клінічних дослідженнях з
метою порівняння рекомбінантного людського ФСГ (р-лФСГ) (фолітропіну
альфа) та сечового ФСГ при проведенні процедур допоміжних репродуктивних
технологій (ДРТ) (див. таблицю 1) та індукції овуляції фолітропін альфа
виявився ефективнішим, ніж сечовий ФСГ, що виражалося у нижчій
загальній дозі та коротшому періоді лікування, необхідних для індукції
дозрівання фолікула. Застосування нижчих доз фолітропіну альфа впродовж
коротшого періоду лікування при проведенні ДРТ дало змогу отримати
більшу кількість яйцеклітин, ніж у разі застосування сечового ФСГ.
Таблиця 1
Результати
дослідження GF 8407 (рандомізованого дослідження у паралельних групах з
метою порівняння ефективності та безпеки фолітропіну альфа та сечового
ФСГ у разі застосування допоміжних репродуктивних технологій)
| | Фолітропін альфа (n = 130) | Сечовий ФСГ (n = 116) | |
| 11,0 ± 5,9 | 8,8 ± 4,8 | |
| Необхідна кількість днів стимуляції у разі застосування ФСГ | 11,7 ± 1,9 | 14,5 ± 3,3 | |
| Необхідна загальна доза ФСГ (кількість ампул ФСГ по 75 МО) | 27,6 ± 10,2 | 40,7 ± 13,6 | |
| Необхідність збільшення дози (%) | 56,2 | 85,3 |
Різниця між 2 групами була статистично значущою (p < 0,05) щодо усіх перелічених критеріїв.
Клінічна ефективність та безпека застосування для чоловіків
У
чоловіків з недостатністю ФСГ одночасне застосування фолітропіну альфа
та лХГ упродовж щонайменше 4 місяців сприяє індукуванню сперматогенезу.
Фармакокінетика.
Після
внутрішньовенного введення фолітропін альфа розподіляється у
міжклітинній рідині з початковим періодом напіввиведення, що становить
приблизно 2 години, і виводиться з організму з кінцевим періодом
напіввиведення, що становить приблизно 1 добу. Рівноважний об’єм
розподілу та загальний кліренс становлять 10 л та 0,6 л/год відповідно.
Одна восьма дози фолітропіну альфа виводиться з сечею.
Після
підшкірного введення абсолютна біодоступність фолітропіну альфа
становить близько 70 %. Повторне введення призводить до збільшення його
кумуляції втричі з досягненням рівноважного стану впродовж 3–4 днів. У
жінок з пригніченою секрецією ендогенних гонадотропінів тим не менше
було виявлено, що фолітропін альфа ефективно стимулює фолікулярний
розвиток та стероїдогенез, незважаючи на невимірно низькі рівні ЛГ.
Показання
Дорослі жінки
Ановуляція (включаючи синдром полікістозних яєчників (СПКЯ)) у жінок,
які виявилися нечутливими до лікування кломіфену цитратом.
Стимуляція розвитку множинних фолікулів у пацієнток при проведенні
суперовуляції у рамках допоміжних репродуктивних технологій (ДРТ), таких
як екстракорпоральне запліднення (ЕКЗ), перенесення гамети до
фаллопієвої труби (GIFT) та перенесення зиготи до фаллопієвої труби
(ZIFT).
Фолітропін альфа у комбінації з препаратами
лютеїнізуючого гормону (ЛГ) рекомендується для стимуляції розвитку
фолікулів у жінок з тяжкою недостатністю ЛГ та ФСГ. У клінічних
дослідженнях такі пацієнтки визначалися за рівнем ендогенного
сироваткового ЛГ < 1,2 МО/л.
Дорослі чоловіки
Фолітропін альфа призначений для стимуляції сперматогенезу у чоловіків
із вродженим або набутим гіпогонадотропним гіпогонадизмом, одночасно з
терапією людським хоріонічним гонадотропіном (лХГ).
Протипоказання
Гіперчутливість до діючої речовини або будь-якої з допоміжних речовин (див. розділ «Склад»);
пухлини гіпоталамуса або гіпофіза;
збільшення розміру яєчників або кісти яєчників, не пов’язані із синдромом полікістозних яєчників;
гінекологічні кровотечі невідомого походження;
рак яєчників, матки або молочних залоз.
Фолітропін альфа не можна застосовувати у випадках, коли неможливо отримати ефективну відповідь на лікування, наприклад при:
первинній недостатності яєчників;
вадах статевих органів, несумісних з вагітністю;
фіброзних пухлинах матки, несумісних з вагітністю;
первинній тестикулярній недостатності.
Взаємодія з іншими лікарськими засобами та інші види взаємодії
Одночасне
застосування фолітропіну альфа з іншими лікарськими засобами, що
застосовуються для стимуляції овуляції (наприклад, лХГ, кломіфену
цитрат), може посилювати фолікулярну реакцію, тоді як одночасне
застосування з агоністами або антагоністами
гонадотропін-рилізинг-гормону (ГнРГ), що індукують десенсибілізацію
гіпофіза, може призвести до необхідності збільшення дози фолітропіну
альфа, потрібного для досягнення адекватної реакції яєчників. Про жодні
інші клінічно значущі лікарські взаємодії під час терапії фолітропіном
альфа не повідомлялося.
Особливості щодо застосування
Відстеження
З
метою покращення відстеження біологічних лікарських засобів та
повідомлення про підозрювані побічні реакції медичним працівникам слід
чітко записати торговельну назву та номер партії введеного препарату у
медичну карту пацієнта.
Оскільки фолітропін альфа проявляє значну
гонадотропну активність, яка здатна спричинити розвиток побічних
реакцій від легкого до тяжкого ступенів, препарат можуть призначати лише
лікарі, добре обізнані з проблемами безпліддя та методами його
лікування.
Терапія гонадотропінами потребує витрат певного часу
від лікарів та інших медичних працівників, а також наявності відповідної
апаратури для моніторингу лікування. Безпечне та ефективне застосування
фолітропіну альфа для жінок передбачає регулярний моніторинг
оваріальної реакції за допомогою ультразвукового дослідження, окремо
або, переважно, в поєднанні з одночасним регулярним визначенням
сироваткового рівня естрадіолу. Можлива певна індивідуальна
варіабельність відповіді на застосування ФСГ, тобто у одних пацієнтів
може відзначатися слабка реакція на ФСГ, а у інших – надмірна. Для
лікування як жінок, так і чоловіків варто застосовувати найнижчу
ефективну дозу препарату відповідно до мети лікування.
Порфірія
Під
час лікування фолітропіном альфа пацієнти з порфірією або з випадками
порфірії у сімейному анамнезі повинні перебувати під ретельним медичним
наглядом. При перших ознаках розвитку цього стану або при його
погіршенні може виникнути потреба у припиненні лікування.
Лікування жінок
Перед
початком лікування необхідно ретельно дослідити причину безпліддя пари
та визначити можливі протипоказання до вагітності. Зокрема, пацієнтів
слід обстежити на наявність гіпотиреозу, недостатності надниркових
залоз, гіперпролактинемії та призначити їм відповідне лікування.
При
проведенні стимуляції росту фолікулів під час лікування ановуляторного
безпліддя або процедур ДРТ у пацієнток може спостерігатися збільшення
розміру яєчників або розвиток гіперстимуляції. Дотримання
рекомендованого дозування та режиму введення фолітропіну альфа, а також
ретельний моніторинг терапії зменшать частоту подібних явищ. Точна
інтерпретація показників розвитку фолікулів та дозрівання потребує
залучення фахівця, який має досвід тлумачення відповідних тестів.
Під
час клінічних досліджень було виявлено посилення чутливості яєчників до
дії фолітропіну альфа при одночасному введенні лютропіну альфа. Якщо
вважається за необхідне збільшення дози ФСГ, коригування дози бажано
здійснювати з інтервалами у 7–14 днів та з покроковим підвищенням на
37,5–75 МО.
Безпосереднього порівняння застосування фолітропіну
альфа/ ЛГ та людського менопаузального гонадотропіну (лМГ) не
проводилося. Порівняння з існуючими даними дає підстави припустити, що
частота овуляцій, отримана при застосуванні фолітропіну альфа/ ЛГ,
подібна до частоти, отриманої для лМГ.
Синдром гіперстимуляції яєчників (СГСЯ)
Очікуваним
наслідком контрольованої стимуляції яєчників є певне їх збільшення. Це
явище, що найбільш поширене у жінок із синдромом полікістозних яєчників,
зазвичай минає без лікування.
На відміну від неускладненого
збільшення розміру яєчників, СГСЯ є синдромом, що проявляється з
наростанням ступеня тяжкості. Він включає значне збільшення розміру
яєчників, високі сироваткові рівні статевих стероїдів та зростання
проникності судин, що може призвести до накопичення рідини в черевній,
плевральній та іноді у перикардіальній порожнинах.
У тяжких
випадках СГСЯ можуть спостерігатися такі симптоми: біль і відчуття
розтягнення у черевній порожнині, значне збільшення розміру яєчників,
збільшення маси тіла, задишка, олігурія та симптоми з боку
шлунково-кишкового тракту, включаючи нудоту, блювання та діарею. При
клінічному обстеженні можуть бути виявлені гіповолемія,
гемоконцентрація, електролітний дисбаланс, асцит, гемоперитонеум,
плевральні випоти, гідроторакс або гострий респіраторний
дистрес-синдром. У рідкісних випадках тяжкий СГСЯ може бути ускладнений
перекручуванням яєчників та тромбоемболічними явищами, такими як емболія
легеневої артерії, ішемічний інсульт та інфаркт міокарда.
До
незалежних факторів ризику розвитку СГСЯ належать синдром полікістозних
яєчників, високі абсолютні або швидко зростаючі сироваткові рівні
естрадіолу (наприклад > 900 пг/мл або > 3300 пмоль/л при
ановуляції; > 3000 пг/мл або > 11000 пмоль/л при ДРТ) та велика
кількість фолікулів, що формуються (наприклад > 3 фолікулів діаметром
≥ 14 мм при ановуляції; ≥ 20 фолікулів діаметром ≥ 12 мм при ДРТ).
Дотримання
рекомендованого дозування та режиму введення фолітропіну альфа може
мінімізувати ризик оваріальної гіперстимуляції (див. розділи «Спосіб
застосування та дози» та «Побічні реакції»). Для раннього виявлення
відповідних факторів ризику рекомендується проводити моніторинг циклів
стимуляції за допомогою ультразвукового дослідження та визначення рівня
естрадіолу.
Відомо, що лХГ відіграє ключову роль в ініціації СГСЯ
і що цей синдром може ставати тяжчим та тривалішим при настанні
вагітності. Тому за наявності ознак гіперстимуляції яєчників, таких як
сироваткові рівні естрадіолу > 5500 пг/мл або > 20200 пмоль/л
та/або загальна кількість фолікулів ≥ 40, рекомендується відмінити
введення лХГ та порадити пацієнтці утримуватися від статевих зносин або
застосовувати бар’єрні засоби контрацепції впродовж щонайменше 4 днів.
СГСЯ може швидко прогресувати (у межах 24 годин), і протягом кількох
днів стати серйозним медичним ускладненням. Найчастіше він виникає після
припинення гормональної терапії та досягає максимуму приблизно через
7–10 днів після завершення лікування. Тому після введення лХГ пацієнтки
мають перебувати під медичним наглядом щонайменше протягом 2 тижнів.
Частоту розвитку гіперстимуляції при проведенні ДРТ може зменшити аспірація всіх фолікулів до овуляції.
Зазвичай
легкі або помірні форми СГСЯ минають спонтанно. Якщо спостерігається
тяжка форма СГСЯ, лікування гонадотропінами рекомендується припинити,
якщо воно ще продовжується, пацієнтку слід госпіталізувати та розпочати
відповідну терапію.
Багатоплідна вагітність
Частота
багатоплідних вагітностей у разі індукції овуляції вища, ніж після
природного запліднення. Більшість множинних запліднень представлена
двійнями. Багатоплідна вагітність, особливо вищого порядку, несе
підвищений ризик небажаних наслідків для матері, плода та
новонародженого.
Для зниження ризику багатоплідної вагітності рекомендується ретельно контролювати реакцію яєчників.
При
проведенні процедур ДРТ ризик багатоплідної вагітності пов’язаний,
головним чином, з кількістю пересаджених ембріонів, їхньою якістю та
віком пацієнтки.
Пацієнтки мають бути проінформовані про потенційний ризик багатоплідної вагітності до початку лікування.
Переривання вагітності
У
пацієнток при проведенні стимуляції росту фолікулів для індукції
овуляції або ДРТ частота випадків переривання вагітності внаслідок
викидня або спонтанного аборту вища, ніж після природного запліднення.
Позаматкова вагітність
Жінки
із захворюваннями труб в анамнезі мають ризик позаматкової вагітності
незалежно від того, настала вона внаслідок спонтанного запліднення чи
лікування безпліддя. Повідомлялося, що поширеність позаматкової
вагітності після проведення ДРТ вища, ніж у загальній популяції.
Новоутворення органів репродуктивної системи
Існують
повідомлення як про доброякісні, так і про злоякісні новоутворення
яєчників та інших органів репродуктивної системи у жінок, які проходили
різні режими лікування безпліддя. Ще не встановлено, чи збільшує
лікування гонадотропінами ризик розвитку таких пухлин у безплідних
жінок.
Вроджені вади
Поширеність вроджених вад після
проведення ДРТ може бути дещо вищою, ніж після спонтанного запліднення.
Вважається, що це є наслідком характеристик стану здоров’я батьків
(наприклад, вік матері, властивості сперми батька) та багатоплідних
вагітностей.
Тромбоемболічні ускладнення
У жінок з
нещодавніми або існуючими тромбоемболічними захворюваннями та у жінок,
для яких загалом встановлено фактори ризику розвитку тромбоемболічних
явищ, такі як індивідуальні або сімейні випадки, лікування
гонадотропінами може призвести до подальшого зростання ризику
загострення або появи подібних явищ. У таких жінок необхідно оцінити
перевагу застосування гонадотропінів над існуючим ризиком розвитку таких
ускладнень. Проте слід відзначити, що власне вагітність та СГСЯ
збільшують ризик розвитку тромбоемболічних ускладнень.
Лікування чоловіків
Підвищення
ендогенних рівнів ФСГ у пацієнтів є показником первинної тестикулярної
недостатності. Такі пацієнти нечутливі до терапії фолітропіном альфа/
лХГ. Фолітропін альфа не слід застосовувати у випадках, коли неможливо
отримати ефективну відповідь на лікування.
Для оцінки реакції на лікування рекомендується проводити аналіз сім’яної рідини через 4–6 місяців від початку лікування.
Вміст натрію
Лікарський засіб містить менше 1 ммоль натрію (23 мг) в одній дозі, тобто практично не містить натрію.
Застосування у період вагітності або годування груддю.
Вагітність
Показань
до застосування фолітропіну альфа у період вагітності немає. Дані,
отримані для невеликої кількості випадків застосування препарату у
період вагітності (менше 300 випадків), свідчать про відсутність
вроджених вад або фето/неонатальної токсичності фолітропіну альфа.
У
дослідженнях на тваринах тератогенного ефекту не спостерігалося.
Клінічних даних для виключення тератогенного ефекту фолітропіну альфа
при застосуванні його під час вагітності недостатньо.
Годування груддю
Фолітропін альфа не показаний для застосування у період годування груддю.
Фертильність
Фолітропін альфа показаний для лікування безпліддя (див. розділ «Показання»).
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
Очікується, що фолітропін альфа не впливає або майже не впливає на здатність керувати автомобілем та працювати з механізмами.
Спосіб застосування та дози
Лікарський
засіб Бемфола призначений для підшкірного введення. Першу ін’єкцію
лікарського засобу слід проводити під безпосереднім наглядом медичного
працівника.
Самостійне введення лікарського засобу можуть
проводити лише добре мотивовані, належним чином навчені пацієнти, які у
разі необхідності мають можливість проконсультуватися з фахівцем.
Попередньо
наповнена ручка, що містить картридж з разовою дозою лікарського засобу
Бемфола, призначений для одноразового застосування. Отже, пацієнти
мають отримати чіткі інструкції, щоб не допустити неправильного
застосування одноразового пристрою.
РЕКОМЕНДАЦІЇ ДЛЯ САМОСТІЙНОГО ВВЕДЕННЯ ЛІКАРСЬКОГО ЗАСОБУ БЕМФОЛА ЗА ДОПОМОГОЮ ГОТОВОЇ ДО ЗАСТОСУВАННЯ РУЧКИ ДЛЯ ВВЕДЕННЯ
Попередження:
будь-ласка, уважно прочитайте інструкцію перед самостійним
застосуванням ручки для введення з препаратом Бемфола. Не дотримуйтесь
вказівок з інших джерел, окрім тих, які наведено в цій інструкції для
медичного застосування, або вказівок вашого лікаря, оскільки це може
поставити під загрозу правильне використання попередньо наповненої ручки
та ваше лікування.
1. Як користуватися попередньо наповненою ручкою з препаратом Бемфола
Повністю прочитайте інструкцію перед застосуванням попередньо наповненої ручки.
Кожна попередньо наповнена ручка призначена лише для вашого використання, не дозволяйте іншим людям користуватися нею.
Цифри на дисплеї попередньо наповненої ручки означають дозу препарату в
міжнародних одиницях (МО). Лікар скаже Вам, скільки МО Вам необхідно
вводити щодня.
;Ваш лікар/фармацевт розкаже Вам, скільки
попередньо наповнених ручок для введення з препаратом Бемфола Вам
необхідно буде використати впродовж повного курсу лікування.
Робіть собі ін’єкцію щодня у той самий час.
2. Перед застосуванням попередньо наповненої ручки:
2.1. Дістаньте ручку з холодильника
Дістаньте одну з Ваших ручок для введення із холодильника за 5–10 хвилин до її використання.
Якщо препарат заморожений, будь ласка, не використовуйте його.
2.2. Вимийте руки
Вимийте Ваші руки теплою водою з милом та висушіть їх.
Важливо, щоб Ваші руки та все, що Ви будете використовувати при підготовці ручки для введення, були якомога чистішими.
2.3. Оберіть чисте місце
Підходящим місцем може бути чистий стіл або інша поверхня.
2. Підготовка попередньо наповненої ручки до ін’єкції
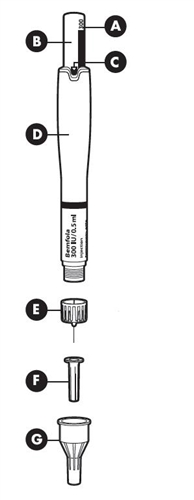
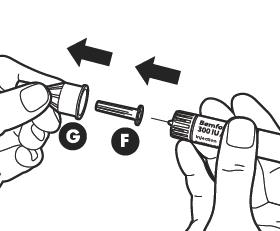
Різні частини попередньо наповненої ручки
| A – дозатор; B – регулятор дози; C – стрічка активації; D – картридж з лікарським засобом; E – голка; F – внутрішній ковпачок голки; G – зовнішній ковпачок голки
|
|
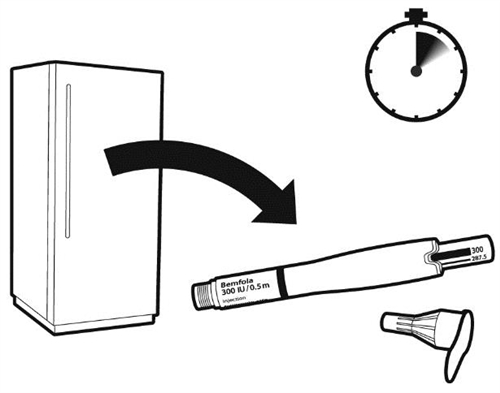
| Робіть ін’єкцію щодня приблизно у той самий час. Дістаньте ручку для введення з холодильника за 5–10 хвилин до її застосування. Примітка: переконайтеся, що препарат не заморожений.
|
|
| Підготуйте голку для ін’єкції Дістаньте нову голку. Використовуйте тільки одноразові голки, які входять в комплект упаковки. Міцно тримайте зовнішній ковпачок голки. У всіх випадках перевіряйте, щоб етикетка контролю розкривання не була пошкоджена чи ослаблена. Зніміть з голки для ін’єкцій етикетку контролю розкривання. Увага: якщо етикетка контролю розкривання пошкоджена або ослаблена, не використовуйте голку. Викиньте її в контейнер для утилізації гострих предметів. Візьміть нову голку.
|
|
| Прикріпіть голку. Тримаючи ручку з боків і голку на одній лінії з ручкою, приєднайте голку і щільно зафіксуйте її на кінчику ручки. Переконайтеся, що голка правильно закріплена на ручці в прямому положенні. Увага: незважаючи на те, що на кінці ручки є різьба, ніколи не намагайтеся прикрутити голку до ручки, оскільки це може призвести до неправильного положення голки Не натискайте на регулятор дози під час приєднання голки.
|
|
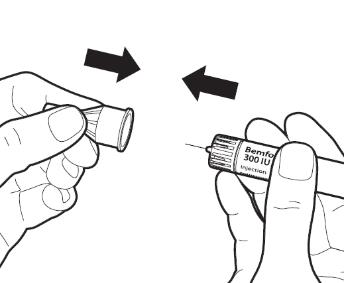
| Зніміть зовнішній ковпачок голки (G). Зберігайте ковпачок ‒ він Вам знадобиться після ін’єкції, щоб викинути ручку.
Зніміть внутрішній ковпачок голки (F).
Переконайтеся, що голка знаходиться в правильному положенні.
|
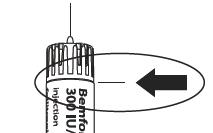
| Правильне положення голки
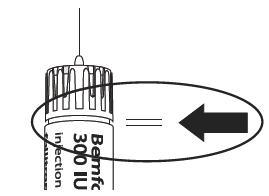
| Неправильне положення голки
|
|
4. Встановлення дози, яка призначена вашим лікарем | |
|
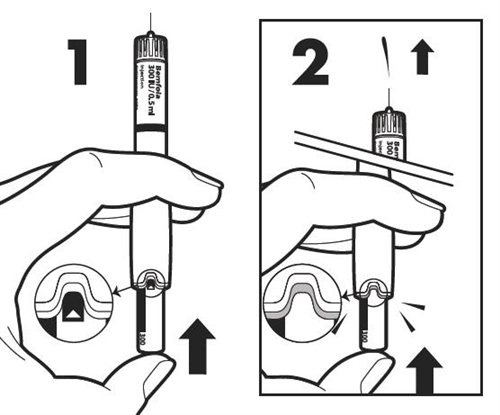
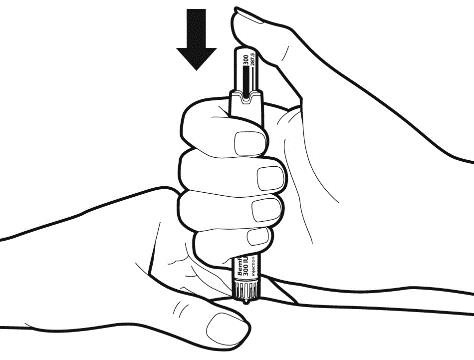
| Спочатку тримайте ручку для введення голкою догори. Щоб видалити повітряні бульбашки з системи, легенько постукайте по боковій поверхні ручки, щоб можливі повітряні бульбашки піднялися вгору.
|
|
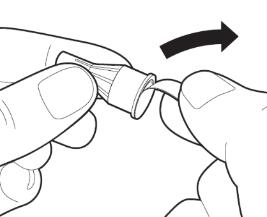
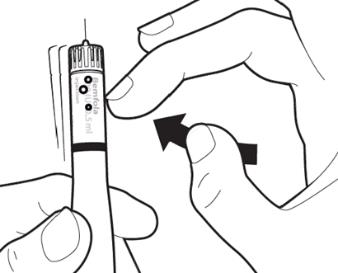
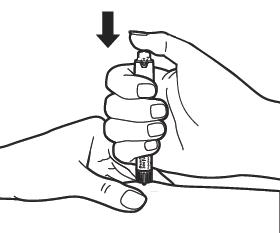
| Тримаючи ручку для введення голкою догори, натисніть на регулятор дози, доки не зникне стрічка активації з маленькою стрілкою. Ви також почуєте клацання і невелика кількість рідини вивільниться з голки (це нормально). Тепер ручка готова для встановлення дози.
Увага: якщо рідина не виприсне або на стику голки та ручки виявиться витік рідини, ручку для введення застосовувати неможна. Повідомте свого лікаря або фармацевта, якщо ви помітили будь-які проблеми.
|
|
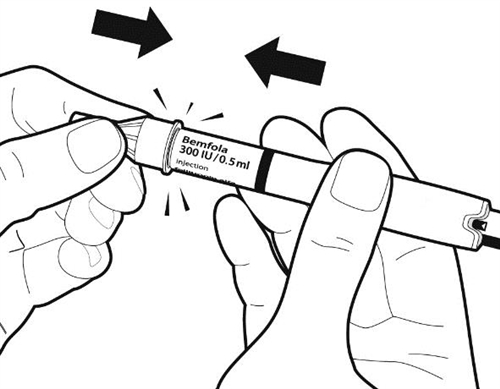
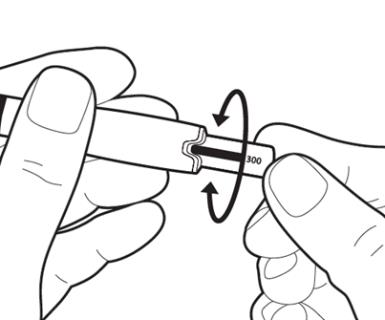
| Обережно повертайте регулятор дози, доки показник призначеної Вам дози не з’явиться на одній лінії з серединою виступу на ручці. Примітка: у попередньо наповненій ручці з дозуванням 75 МО/0,125 мл регулятор дози не можна повернути повністю, але його можна повертати в зворотному напрямку. Тепер ручка для введення готова до ін’єкції. Увага: не натискайте на регулятор дози в даний момент. |
| 5. Введення дози Тепер Ви готові для негайного введення ін'єкції. Ваш лікар або медсестра вже порадили Вам, у яку ділянку тіла робити ін’єкцію (наприклад живіт, передня поверхня стегна). Щоб мінімізувати подразнення шкіри, кожного дня обирайте інше місце для ін’єкції. | |
|
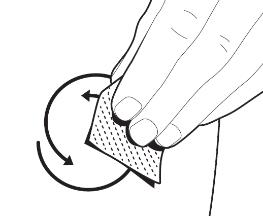
| Круговими рухами протріть шкіру у місці ін’єкції серветкою, просоченою спиртом, яка знаходиться в упаковці. Зачекайте кілька секунд, поки спирт не випарується зі шкіри і вона підсохне, перш ніж робити ін’єкцію. |
|
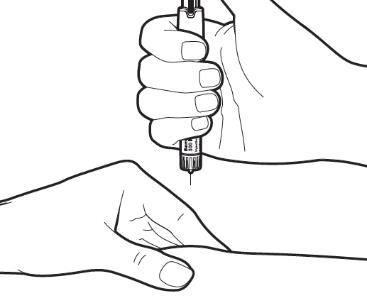
| Переконайтеся ще раз, що правильна доза відображається на ручці. Обережно зберіть у складку шкіру ділянки ін'єкції. Тримайте ручку приблизно під прямим кутом (кут 90º) і повністю введіть голку в шкіру одним рівномірним рухом. Увага: не натискайте на регулятор дози під час введення голки та не змінюйте напрямок голки при введенні в шкіру.
|
|
| Після того, як голка повністю введена в місце ін’єкції, натискайте регулятор дози повільно і безперервно до упору, доки індикатор встановленої дози не зникне. Не виймайте голку відразу, зачекайте принаймні 5 секунд, перш ніж витягнути її, щоб переконатися, що ви ввели повну дозу. Витягнувши голку, круговими рухами протріть шкіру спиртовою серветкою. Увага: якщо під час ін’єкції на стику голки та ручки виявлено витік рідини, повідомте про це свого лікаря або фармацевта.
|
| 6. Після ін’єкції | |
|
| Обережно надягніть на голку зовнішній ковпачок. |
|
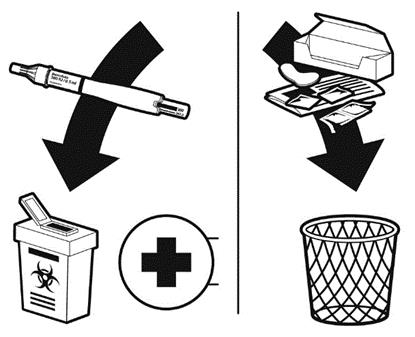
| Попередньо наповнену ручку можна використати лише один раз. Її потрібно викинути, навіть якщо після ін’єкції в ручці залишилася рідина. Викиньте у смітник упаковку, внутрішній ковпачок голки, наклейку, спиртову серветку та Інструкцію для медичного застосування. Не викидайте лікарські засоби в раковину, туалет або побутовий смітник. Використану ручку необхідно помістити в контейнер для гострих предметів і повернути до медичного закладу для правильної утилізації. Запитайте свого фармацевта, як розпоряджатися лікарським засобом, яким Ви більше не користуєтесь. |
Примітка: протягом терміну придатності закритий лікарський засіб може зберігатися при температурі не вище 25 ºС протягом 3 місяців без повторного охолодження; лікарський засіб слід утилізувати, якщо він не був використаний по закінченню 3 місяців.
Діти.
Відповідних показань для застосування фолітропіну альфа пацієнтам педіатричної групи немає.
Передозування
Прояви
передозування фолітропіном альфа невідомі, проте існує можливість
розвитку синдрому гіперстимуляції яєчників (див. розділ «Особливості
застосування»).
Побічні ефекти
Резюме профілю безпеки.
Найпоширенішими
побічними реакціями є головний біль, кісти яєчників та місцеві реакції у
місці введення (наприклад, біль, еритема, гематома, набряк та/або
подразнення у місці ін’єкції).
Часто повідомлялося про випадки
синдрому гіперстимуляції яєчників (СГСЯ) легкого або помірного ступеня
тяжкості, який слід вважати невід’ємним ризиком процедури стимуляції.
Тяжкі форми СГСЯ нечасті (див. розділ «Особливості застосування»).
Дуже рідко можуть траплятися випадки тромбоемболії (див. розділ «Особливості застосування»).
Для визначення частоти побічних реакцій використовують такі критерії:
Дуже часті (≥ 1/10, виникають більше ніж у 1 з 10 осіб).
Часті (від ≥ 1/100 до < 1/10, виникають не більше ніж у 1 з 10 осіб).
Нечасті (від ≥ 1/1000 до < 1/100, виникають не більше ніж у 1 зі 100 осіб).
Поодинокі (від ≥ 1/10000 до < 1/1000, виникають не більше ніж у 1 з 1 000 осіб).
Рідкісні (< 1/10000, виникають менше ніж у 1 з 10 000 осіб).
Лікування жінок
З боку імунної системи
Рідкісні: реакції гіперчутливості від легкого до тяжкого ступеня, включаючи анафілактичні реакції та шок.
З боку нервової системи
Дуже часті: головний біль.
Судинні розлади
Рідкісні: тромбоемболія (як у поєднанні із СГСЯ, так і окремо).
З боку дихальної системи, органів грудної клітки та середостіння
Рідкісні: загострення або погіршення астми.
З боку травної системи
Часті: біль у животі, відчуття розтягнення та дискомфорту у черевній порожнині, нудота, блювання, діарея.
З боку репродуктивної системи та молочних залоз
Дуже часті: кісти яєчників.
Часті: СГСЯ від легкого до помірного ступеня тяжкості (включаючи супутні симптоми).
Нечасті: тяжкий СГСЯ (включаючи супутні симптоми) (див. розділ «Особливості застосування»).
Поодинокі: ускладнення тяжкого СГСЯ.
Загальні розлади та реакції у місці введення
Дуже часті: реакції у місці ін’єкції (наприклад біль, еритема, гематома, набряк та/або подразнення у місці ін’єкції).
Лікування чоловіків
З боку імунної системи
Рідкісні: реакції гіперчутливості від легкого до тяжкого ступеня, включаючи анафілактичні реакції та шок.
З боку дихальної системи, органів грудної клітки та середостіння
Рідкісні: загострення або погіршення астми.
З боку шкіри та підшкірних тканин
Часті: акне.
З боку репродуктивної системи та молочних залоз
Часті: гінекомастія, варикоцеле.
Загальні розлади та реакції у місці введення
Дуже часті: реакції у місці ін’єкції (наприклад біль, еритема, гематома, набряк та/або подразнення у місці ін’єкції).
Лабораторні та інструментальні дані
Часті: збільшення маси тіла.
Повідомлення про підозрювані побічні реакції
Повідомлення
про підозрювані побічні реакції лікарського засобу мають велике
значення. Вони дають змогу продовжувати моніторинг співвідношення
користь/ризик лікарського засобу. Медичних працівників просять
повідомляти про будь-які підозрювані побічні реакції, використовуючи
національну систему інформування. Медичним працівникам слід впевнитись,
що торгова назва та номер серії лікарського засобу зазначені у
повідомлені про підозрювану побічну реакцію.
Термін придатності
3 роки.
Після відкриття лікарський засіб слід вводити негайно.
Не застосовувати після закінчення терміну придатності, зазначеного на упаковці.
Умови зберігання
Зберігати у холодильнику (2–8 ºС). Не заморожувати.
До
відкриття протягом терміну придатності закритий лікарський засіб може
зберігатися не в холодильнику при температурі не вище 25 ºС протягом 3
місяців без повторного охолодження. Лікарський засіб слід утилізувати,
якщо він не був використаний протягом
3 місяців.
Зберігати в оригінальній упаковці для захисту від світла.
Зберігати у недоступному для дітей місці.
Несумісність
Не застосовується.
Упаковка
По
0,125 мл або 0,25 мл, або 0,375 мл, або 0,50 мл, або 0,75 мл розчину
для ін'єкцій в скляному картриджі, з гумовою пробкою-поршнем і гумовим
диском з алюмінієвим ковпачком, вміщеному у ручку для введення. По 1 або
5, або 10 попередньо наповнених ручок з одноразовими голками
(відповідно 1 або 5 або 10) і серветками, просоченими спиртом
(відповідно 1 або 5 або 10) разом з інструкцією для медичного
застосування у картонній коробці.
Категорія відпуску
За рецептом.
Виробник
ВАТ «Гедеон Ріхтер».
Місцезнаходження виробника та адреса місця провадження його діяльності.
Н-1103, Будапешт, вул. Демреї, 19-21, Угорщина.
| Особливості | |
| Країна: | Угорщина |
| Рецептурний: | Рецепт |
| Номер реєстрації: | UA/17528/01/01 |
| Штрих код: | 5 997 001 367 216 |